一つの世界の戦い
─Covid-19パンデミックの課題に対応する共通の運命のグローバルコミュニティを構築するための国際協力
世界中を掃除する小説コロナウイルスは、継続的な世界的なCovid-19のパンデミック危機をもたらしました。小説のコロナウイルスには国境がなく、Covid-19とのこの戦いから免れる国はありません。この世界的なCovid-19パンデミックに対応して、Liming Bio-Products Corpは、グローバルコミュニティの幸福を支援するために貢献しています。
私たちの世界は現在、新しいコロナウイルス病2019(Covid-19)パンデミックの前例のない影響に直面しています。現在までに、この病気の治療に利用できる効率的な薬はありません。ただし、Covid-19の検出のために多くの診断テストが開発されています。これらのテストは、新しいコロナウイルス特異的核酸または抗体バイオマーカーを検出するための分子または血清学的方法に基づいています。 Covid-19がパンデミックの状態に達したため、ウイルスの拡散を評価して含む際に、新しいコロナウイルス感染の早期診断が重要ですが、普遍的な使用のための完全なテストはまだ存在しません。 Covid-19感染のスクリーニング、診断、および監視に使用できる可能性があり、それらの制限は何であるかを知る必要があります。これらの科学的ツールをより適切に活用し、この急速に広がって深刻な病気の出現を特定して制御する方法が非常に重要です。
新規コロナウイルスの検出の目的は、Covid-19感染を抱えている個人か、黙ってウイルスを散布する可能性のある漸近運送業者が臨床治療の意思決定を導くための重要な情報を提供するかどうかを判断することです。以前の研究では、臨床決定の70%が検査結果に依存することが示されています。異なる検出方法を使用すると、検出試薬キットの要件も異なります。
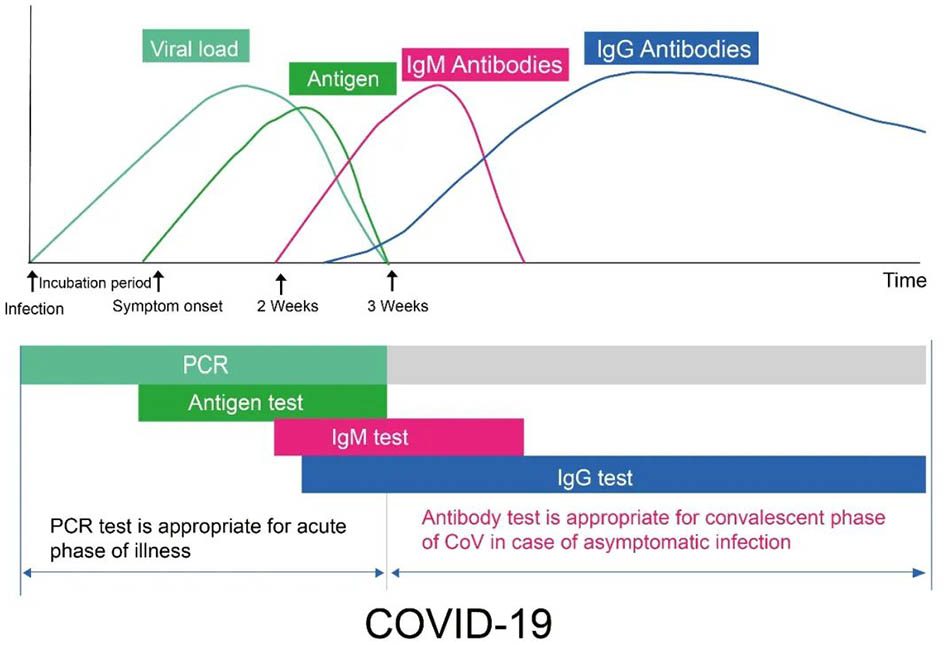
図1
図1:Covid-19感染の典型的な時間経過における一般的なバイオマーカーレベルの重要な段階を示す図。 X軸は感染症の日数を示し、Y軸は異なる期間におけるウイルス量、抗原の濃度、抗体の濃度を示します。抗体とは、IgMおよびIgG抗体を指します。 RT-PCRと抗原検出の両方を使用して、初期の患者検出の直接的な証拠である新しいコロナウイルスの有無を検出するために使用されます。ウイルス感染から1週間以内に、PCR検出、または抗原検出が推奨されます。約7日間の新規コロナウイルス感染の後、新規コロナウイルスに対するIgM抗体は患者の血液で徐々に増加しましたが、存在の期間は短く、その濃度は急速に減少します。対照的に、ウイルスに対するIgG抗体は、通常ウイルス感染の約14日後に後で現れます。 IgG濃度は徐々に増加し、血液中は長期にわたって持続します。したがって、IGMが患者の血液で検出された場合、それはウイルスが最近感染していることを意味します。これは早期感染マーカーです。 IgG抗体が患者の血液で検出されると、ウイルス感染がしばらくの間であったことを意味します。また、後期感染または以前の感染とも呼ばれます。回復段階にいる患者でよく見られます。
新しいコロナウイルスのバイオマーカー
新規コロナウイルスはRNAウイルスであり、タンパク質と核酸で構成されています。ウイルスは宿主(ヒト)体に侵入し、対応する受容体ACE2に結合部位を介して細胞に入り、宿主細胞で複製し、ヒト免疫系が外来侵略者に応答し、特定の抗体を産生します。したがって、バイアル核酸と抗原、および新規コロナウイルスに対する特定の抗体は、理論的には、新規コロナウイルスの検出のための特定のバイオマーカーとして使用できます。核酸検出の場合、RT-PCRテクノロジーが最も一般的に使用されていますが、血清学的方法は一般的に新規コロナウイルス特異的抗体の検出に使用されます。現在、Covid-19感染をテストするために選択できるさまざまなテスト方法があります[1]。
新規コロナウイルスの主要な試験方法の基本原則
これまでのところ、COVID_19の多くの診断テストが利用可能であり、毎日緊急使用許可の下でより多くのテストキットが承認を受けています。非常に多くの異なる名前と形式で発表される新しいテスト開発は、現在のCOVID_19テストのすべてが基本的に2つの主要な技術に依存しています:ウイルスRNAの核酸検出とウイルス特異的抗体(IGMおよびIGG)を検出する血清学的免疫アッセイ。
01。核酸検出
逆転写 - ポリメラーゼ連鎖反応(RT-PCR)、ループを介した等温増幅(LAMP)、および次世代シーケンス(NGS)は、新規コロナウイルスRNAの検出のための一般的な核酸法です。 RT-PCRは、Covid-19の最初のタイプのテストであり、世界保健機関(WHO)と米国疾病管理予防センター(CDC)の両方が推奨しています。
02.セロロジー抗体検出
抗体は、ウイルス感染に応じて人体で産生される保護タンパク質です。 IgMは初期のタイプの抗体であるのに対し、IgGは後のタイプの抗体です。血清または血漿サンプルは通常、Covid-19感染の急性および回復期の相の評価のために、特定のIgMおよびIgGタイプの抗体の存在について調べられます。これらの抗体ベースの検出方法には、コロイド金免疫クロマトグラフィーアッセイ、ラテックスまたは蛍光ミクロスフェア免疫クロマトグラフィー、酵素結合免疫吸着アッセイ(ELISA)、および化学発光アッセイが含まれます。
03.ウイルス抗原検出
抗原は、免疫防御システムを引き起こす人体によって認識されるウイルス上の構造であり、血液や組織からウイルスを除去するための抗体を産生します。ウイルスに存在するウイルス抗原は、免疫測定法を使用して標的と検出できます。ウイルスRNAと同様に、ウイルス抗原も感染した人の呼吸器に存在し、Covid-19感染の急性期の診断に使用できます。したがって、初期の抗原試験のために、唾液、鼻咽頭、中咽頭スワブ、深部咳止め、気管支肺胞洗浄液(BALF)などの上気道標本を収集することをお勧めします。
新しいコロナウイルスのテスト方法の選択
テスト方法の選択には、臨床設定、品質管理のテスト、ターンアラウンド時間、テストコスト、収集方法のサンプリング、実験室の人員の技術要件、施設および機器の要件など、多くの要因が含まれます。核酸またはウイルス抗原の検出は、ウイルスの存在の直接的な証拠を提供し、新しいコロナウイルス感染の診断を確認することです。抗原検出には多くの方法がありますが、新規コロナウイルスの検出感度は、RT-PCR増幅のそれよりも理論的には低いです。抗体検査は、人体で産生される抗ウイルス抗体の検出であり、時間内に遅れており、ウイルス感染の急性期に早期に検出するために使用できないことがよくあります。検出アプリケーションの臨床設定は異なる場合があり、サンプル収集部位も異なる場合があります。ウイルス核酸と抗原の検出のために、標本は、鼻咽頭スワブ、中咽頭スワブ、sp、または気管支肺胞洗浄液(BALF)など、ウイルスが存在する呼吸管に収集する必要があります。抗体ベースの検出のために、血液標本を収集し、特定のウイルス剤抗体(IgM/IgG)の存在を調べる必要があります。ただし、抗体および核酸テストの結果は互いに補完する可能性があります。たとえば、検査結果が核酸陰性、IgM陰性であるがIgG陽性である場合、これらの結果は、患者が現在ウイルスを運んでいないが、新規コロナウイルス感染から回収されたことを示しています。 [2]
新しいコロナウイルステストの利点と短所
新規コロナウイルス肺炎の診断と治療プロトコル(試験版7)(2020年3月3日に国民保健委員会および伝統的漢方医学の州管理が発表)は、小説の診断のためのゴールドスタンダード方法として使用されますコロナウイルス感染は、抗体検査も診断の確認方法の1つと見なされます。

病原性および血清学的所見
(1)病原性発見:RT-PCRAND/またはNGS法を使用して、鼻咽頭スワブ、sp、sput、下気道分泌、血液、糞、およびその他の標本で、新規コロナウイルス核酸を検出できます。標本が下気道(sputまたは大気抽出)から得られる場合、より正確です。標本は、収集後できるだけ早くテスト用に提出する必要があります。
(2)血清学的所見:NCPウイルス固有のIGMは、発症後約3〜5日後に検出可能になります。 IgGは、急性期と比較して回復期の少なくとも4倍の増加の滴定に達します。
ただし、テスト方法の選択は、地理的な場所、医療規制、臨床環境に依存します。米国では、NIHがコロナウイルス疾患2019(Covid-19)治療ガイドライン(サイト更新:2020年4月21日)を発行し、FDAは公衆衛生緊急事態(2020年3月16日に発行されたコロナウイルス疾患-2019の診断テストに関するポリシーを発行しました。 )、スクリーニングテストとしてのみ選択されたIgM/IgG抗体の血清学的検査。
核酸検出方法
RT_PCRは、新規コロナウイルスRNAが呼吸器または他の標本に存在するかどうかを検出するために設計された非常に敏感な核酸テストです。陽性のPCRテスト結果は、Covid-19感染を確認するために、サンプルに新規コロナウイルスRNAが存在することを意味します。負のPCRテスト結果は、サンプルの品質が低い、または回復された段階での病気の時点などの影響を受ける可能性があるため、ウイルス感染がないことを意味するものではありません。 RT-PCRは非常に敏感なテストですが、いくつかの欠点があります。 RT-PCRテストは、労働集約的で時間がかかり、サンプルの高品質に大きく依存する可能性があります。ウイルスRNAの量は、患者によって異なるだけでなく、サンプルが収集されたときの時点と感染相または臨床症状の発症に応じて同じ患者内で変化する可能性があるため、これは課題になる可能性があります。新しいコロナウイルスを検出するには、十分な量の無傷のウイルスRNAを含む高品質の標本が必要です。
RT-PCRテストは、COVID-19感染症の一部の患者に誤った負の結果(偽陰性)を与える可能性があります。私たちが知っているように、新規コロナウイルスの主な感染部位は、肺と肺胞や気管支などの下気道に位置しています。したがって、深い咳または気管支肺胞洗浄液(BALF)からのsput標本は、ウイルス検出に対して最高の感度を持っていると考えられています。しかし、臨床診療では、鼻咽頭または中咽頭の綿棒を使用することにより、サンプルが上気道から収集されることがよくあります。これらの標本を収集することは、患者にとって不快であるだけでなく、特別に訓練された人員も必要です。サンプリングを侵襲的または簡単にするために、場合によっては、患者に経口スワブを投与され、頬粘膜または舌からサンプルを服用できるようにすることがあります。十分なウイルスRNAがなければ、RT-QPCRは偽陰性テスト結果を返すことができます。中国のHubei州では、最初の検出におけるRT-PCRの感度が約30%〜50%のみであり、平均40%が報告されています。偽陰性の高い割合は、サンプリングが不十分であることによって引き起こされる可能性が最も高い。
さらに、RT-PCRテストでは、複雑なRNA抽出ステップとPCR増幅手順を実行するために、高度に訓練された担当者が必要です。また、より高いレベルのバイオセーフティ保護、特別な実験室施設、リアルタイムPCR機器も必要です。中国では、Biosafetyレベル3(BSL-2)を使用して、Biosafety Level 2 Laboratories(BSL-2)でCOVID-19検出のRT-PCRテストを実行する必要があります。これらの要件の下で、1月の初めから2020年2月上旬まで、中国のWuhanのCDC研究所の能力は、1日あたり数百件しか検出できませんでした。通常、これは他の感染症をテストするときは問題になりません。ただし、Covid-19などの世界的なパンデミックを扱う場合、数百万人の人々がテストされる可能性があるため、RT-PCRは特別な実験室施設または技術機器の要件により重要な問題になります。これらの欠点は、RT-PCRをスクリーニングの効率的なツールとして使用することを制限する可能性があり、テスト結果のレポートの遅延にもつながる可能性があります。
血清学的抗体検出方法
特に中期および後期段階では、病気のコースの進行により、抗体検出率は非常に高くなっています。 Wuhan Central South Hospitalでの研究では、Covid-19感染の第3週に抗体検出率が90%以上に達する可能性があることが示されました。また、抗体は、新規コロナウイルスに対するヒト免疫応答の産物です。抗体検査は、RT-PCRよりもいくつかの利点を提供します。第一に、血清学的抗体はシンプルで迅速で検査されます。抗体横方向のフローテストを使用して、ポイントオブケアに使用して、結果を15分で提供できます。第二に、血清学的検査によって検出された標的は抗体であり、ウイルスRNAよりもはるかに安定していることが知られています。収集、輸送、貯蔵、およびテスト中、抗体検査用の標本は一般に、RT-PCRの標本よりも安定しています。第三に、抗体は血液循環で均等に分布するため、核酸試験と比較してサンプリングの変動は少なくなります。抗体検査に必要なサンプル量は比較的少ないです。たとえば、10マイクロリッキターの指で誘導する血液では、抗体横方向の流れ試験で使用するのに十分です。
一般に、抗体検査は、疾患コース中の新規コロナウイルスの検出率を改善するために、核酸検出のためのサプリメントツールとして選択されます。抗体検査が核酸テストと一緒に使用されると、潜在的な偽陽性および偽陰性の結果を減らすことにより、Covid19の診断のアッセイ精度を高める可能性があります。現在の操作ガイドでは、2種類のテストを独立した検出形式として個別に使用することはお勧めしませんが、組み合わせ形式として使用する必要があります。 [2]
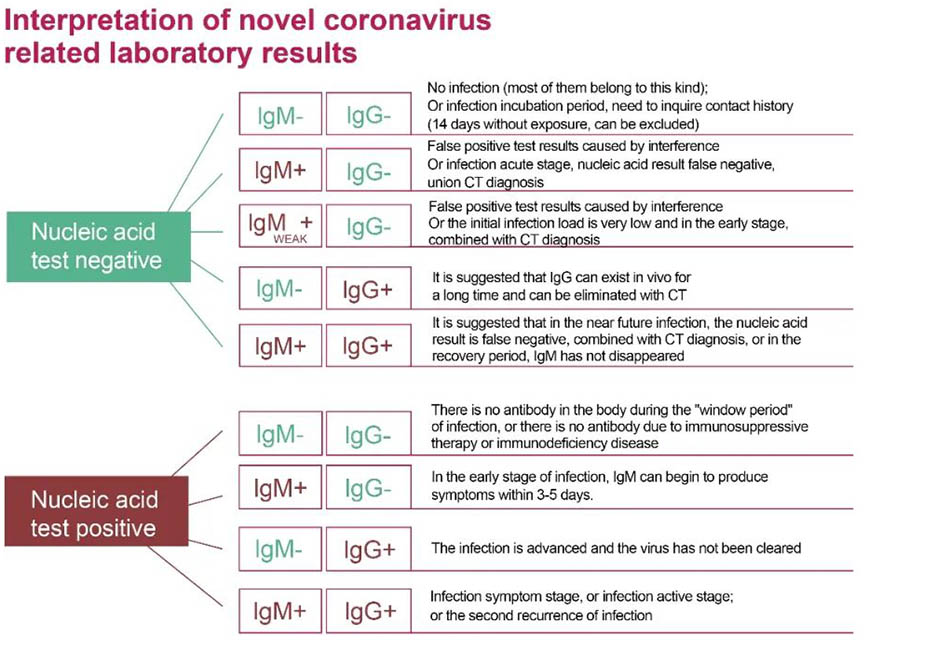
図2:新規コロナウイルス感染の検出のための核酸および抗体検査結果の正しい解釈

図3:Liming Bio-Products Co.、Ltd。 - 新規コロナウイルスIgM/IgG抗体デュアルラピッドテストキット(StrongStep®SARS-COV-2 IgM/IgG抗体迅速検査、ラテックス免疫クロマトグラフィー)

図4:Liming Bio-Products Co.、Ltd。 - StrongStep®新規コロナウイルス(SARS-COV-2)多重リアルタイムPCRキット(3つの遺伝子の検出、蛍光プローブ法)。
注記:この非常に敏感ですぐに使用できるPCRキットは、長期保管のために凍結乾燥形式(凍結乾燥プロセス)で利用できます。キットは室温で輸送および保管でき、1年間安定しています。 Premixの各チューブには、PCR増幅に必要なすべての試薬が含まれています。これには、リバーストランスクリわ角、TAQポリメラーゼ、プライマー、プローブ、DNTPS基質などが含まれます。USERSは、PCRグレードの水とテンプレートを加えて、テンプレートを追加することでミックスを単純に再構成できます。 Amplificationを実行するPCR機器に。
新しいコロナウイルスの発生に応じて、Liming Bio-Products Co.、Ltd。は、臨床および公衆衛生の研究所がCovid-19感染を迅速に診断できるようにするために、2つの診断キットを開発するために迅速に働いてきました。これらのキットは、新しいコロナウイルスの発生が急速に広がっている国や地域での大規模なスクリーニング、およびCovid-19感染の診断と確認を提供するのに非常に適しています。これらのキットは、事前に開拓された緊急使用許可(PEUA)の下でのみ使用するためです。テストは、国または地方自治体の規制に基づいて認定された研究所に限定されています。
抗原検出方法
1。ウイルス抗原検出は、核酸検出と同じ直接検出のカテゴリに分類されます。これらの直接検出方法は、標本のウイルス性病原体の証拠を探し、確認診断に使用できます。ただし、抗原検出キットの開発には、病原性ウイルスを認識および捕捉できる強い親和性と高感度を備えた高品質のモノクローナル抗体が必要です。通常、抗原検出キットの調製に適したモノクローナル抗体を選択および最適化するには6か月以上かかります。
2。現在、新しいコロナウイルスの直接検出のための試薬はまだ研究開発段階にあります。したがって、抗原検出キットは臨床的に検証されており、市販されていません。深Shenzhenの診断会社が抗原検出キットを開発し、スペインで臨床的にテストしたことが以前に報告されていましたが、試薬の質の問題が存在するため、アッセイの信頼性と精度は検証できませんでした。これまで、NMPA(旧中国FDA)は、臨床使用のための抗原検出キットをまだ承認していません。結論として、さまざまな検出方法が開発されました。各方法には利点と制限があります。さまざまな方法の結果を検証と補完に使用できます。
3.高品質のCovid-19テストキットの生産は、研究開発中の最適化に強く依存しています。 Liming Bio-Product Co.、Ltd。テストキットは、厳しい製造および品質管理基準を満たして、最高レベルのパフォーマンスと一貫性を確実に提供するために必要です。 Liming Bio-Product Co.、Ltd。の科学者は、分析的定量化の最高レベルのパフォーマンスを確保するために、in vitro診断キットの設計、テスト、および最適化で20年以上の経験があります。
Covid-19パンデミックの間、中国政府は国際的なホットスポットでの流行予防資料に対する大きな需要の急増に直面しました。 4月5日、国務委員会の共同予防および制御メカニズムの記者会見で、「医療材料の品質管理を強化し、市場の順序を規制する」、江の外国貿易部門の第1レベルの検査官である江のファンである江のファンコマースについて、「次に、最初に、国際社会が必要とするより多くの医療用品の支援を加速し、製品の品質管理、規制、管理を改善するために、2つの側面に努力を集中します。私たちは、世界の流行に共同で対応し、人類の未来を共有するコミュニティを構築することに中国の貢献をします。



図5:Liming Bio-Products Co.、Ltd。の小説コロナウイルス試薬は、EU CE登録証明書を取得しました
名誉証明書


Houshenshan
図6。LimingBio-Products Co.、Ltd。は、Wuhan Vulcan(Houshenshan)Mountain HospitalとCovid-19の流行と戦うために支援し、Wuhan Red Crossの名誉証明書を授与されました。 Wuhan Vulcan Mountain Hospitalは、中国で最も有名な病院であり、重度のcovid -19患者の治療を専門としています。
新しいコロナウイルスの発生が世界中に広がるにつれて、ナンジング・ライミング・バイオ・プロダクト・カンパニーは、この前例のないグローバルな脅威と戦うための革新的な技術を世界中のコミュニティを支援および支援するためにステップアップしています。 Covid-19感染の迅速な検査は、この脅威に対処するための重要な部分です。私たちは、高品質の診断プラットフォームを最前線の医療従事者の手に提供することにより、重要な方法で貢献し続け、人々が必要な重要なテスト結果を受け取ることができます。 Liming Bio-Products Co.、Ltd。のCovid-19パンデミックとの戦いにおける努力は、運命のグローバルコミュニティの建設のための国際コミュニティに技術、経験、専門知識を貢献することです。
ロングプレス〜スキャンしてフォローしてください
メール: sales@limingbio.com
ウェブサイト:https://limingbio.com
投稿時間:5月1日 - 2020年







